La colonscopia di sorveglianza (post-polipectomia)
Il Cancro colorettale (CCR) origina in oltre il 90% dei casi da un precursore locale benigno che è l’adenoma o polipo adenomatoso. L’asportazione endoscopica di tali polipi rappresenta, quindi, la più valida forma di prevenzione del cancro colorettale in quanto interrompe la sequenza adenoma-carcinoma. Ci sono però evidenze che dopo una colonscopia con polipectomia il rischio di formare nuovi adenomi non è annullato per cui il controllo post-polipectomia (colonscopia di sorveglianza) riveste un ruolo strategico nella prevenzione.
Il cancro colorettale (CCR) origina in oltre il 90% dei casi da un precursore locale benigno che è l’adenoma o polipo adenomatoso (Fig. 1). La frequenza degli adenomi segue quella del cancro del colon e, nei paesi occidentali, varia dal 25 al 50% nei soggetti sopra i 50 anni, mentre sono molto rari prima dei 30-40 anni. Considerando che il tempo di transizione da adenoma a cancro è mediamente 10-15 anni, questo ci consente un intervento di diagnosi precoce sulla popolazione.
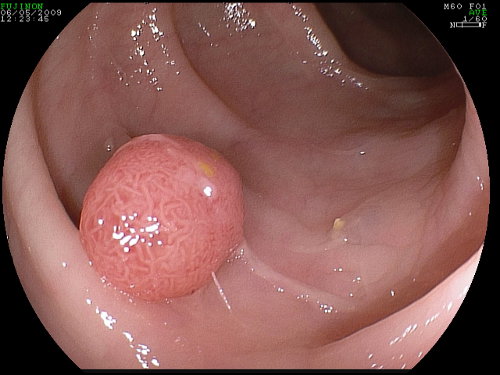
L’asportazione endoscopica di tali polipi rappresenta, quindi, la più valida forma di prevenzione del cancro colorettale in quanto interrompe la sequenza adenoma-carcinoma.
In tale ottica già da anni a livello nazionale ed internazionale sono stati avviati dei programmi di screening, su soggetti sopra i 50 anni e con sangue occulto positivo, con l’intento di individuare e rimuovere gli adenomi, di identificare precocemente le forme tumorali invasive o quelle minimamente invasive che si possono giovare del solo trattamento endoscopico.
Ci sono però evidenze che dopo una colonscopia con polipectomia il rischio di formare nuovi adenomi non è annullato. Anzi, alcuni pazienti possono sviluppare un tumore nei 3-5 anni successivi. In particolare nel 30-50% dei pazienti verranno identificati ulteriori adenomi entro 3 anni, mentre in una percentuale compresa fra 0,3 e 0,9% saranno identificati cancri entro 5 anni.
Nella maggior parte dei casi tali tumori hanno origine da polipi non rimossi completamente o dalla non visualizzazione di piccoli adenomi piatti nel colon destro (per incompleta esplorazione del cieco, toilette intestinale non adeguata, tecnica di esplorazione non corretta, ecc.). E’ molto importante quindi che la prima colonscopia venga eseguita a “regola d’arte” secondo i criteri enunciati dalle Società scientifiche.
Il controllo post-polipectomia (colonscopia di sorveglianza) riveste, quindi, un ruolo importante nella prevenzione del cancro colo rettale e la colonscopia è lo strumento principale di tale prevenzione. Bisogna però tenere conto che si tratta pur sempre di un esame invasivo e come tale può comportare un piccolo rischio di complicanze: perforazione dallo 0,6% (esame diagnostico) al 2% (polipectomia) o emorragia post-polipectomia (0,2.%-2.7% a seconda le dimensioni del polipo asportato). Inoltre, la colonscopia comporta impegno di personale e spese sanitarie non indifferenti. Da ciò si deduce che la colonscopia deve essere indirizzata nei pazienti in cui realmente ci può essere un beneficio e per questo bisogna valutare il potenziale di malignità dei polipi (adenomi) asportati al primo esame che può essere diverso in base al numero, alle dimensioni ed al tipo istologico.
Considerando l’importanza della problematica, il Parlamento Europeo, per tramite un gruppo di specialisti, ha elaborato ed emanato delle linee guida sull’argomento (European guidelines for quality assurance in colorectal cancer screening and diagnosis, 2010) che sono state recepite dalle Società Scientifiche di riferimento.
Per comprendere bene il meccanismo della sorveglianza endoscopica è bene,però, fare prima qualche considerazione di carattere generale sulle caratteristiche dei polipi.
In base alla loro morfologia i polipi adenomatosi sono distinti in sessili e peduncolati e la loro distribuzione rispecchia quella del cancro colo-rettale: Sigma retto 44-53%, Colon discendente/trasverso: 32-36%, Cieco colon/ascendente: 14-20%.
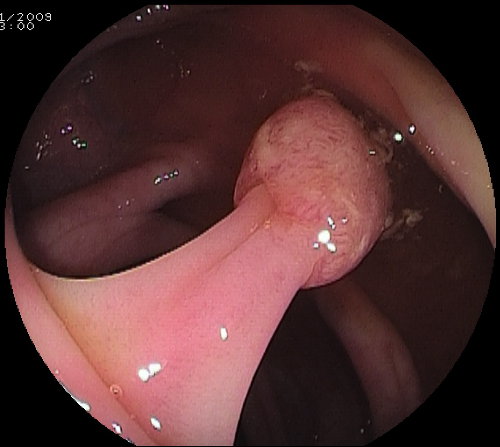
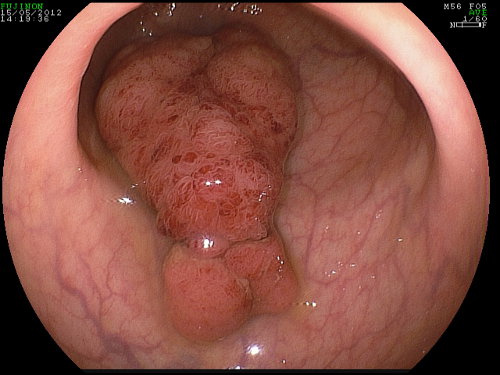
Foto. 2: polipo peduncolato Foto. 3: polipo sessile (di tipo rilevato)
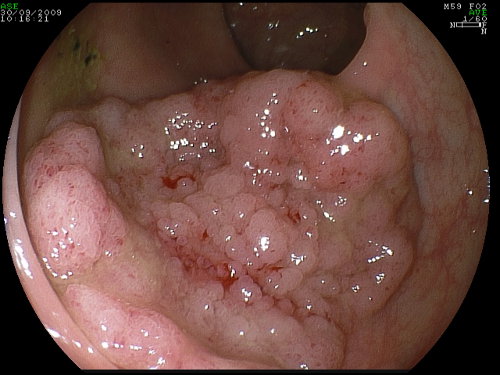
Fig. 4: polipo sessile (di tipo piatto)
In base alla loro istologia i polipi si distinguono in adenomi tubulari, villosi e tubulo-villosi con diverso rischio di trasformazione maligna: 4,8% per gli adenomi tubulari, 22,5% per gli adenomi tubulo-villosi e 40,7% circa per gli adenomi villosi.
Il rischio di trasformazione maligna è legato anche alle dimensioni dei polipi: < 1 cm = rischio uguale a quello della popolazione generale; 1-2 cm = rischio aumentato del 10%; 2 cm = rischio aumentato del 50%.
Sulla base del numero e delle caratteristiche dei polipi alla prima colonscopia è stato così stabilito il successivo controllo endoscopico.
A - Basso rischio (nessuna sorveglianza)
1-2 adenomi inferiori a 10 mm, tubulari e con displasia a basso grado.
B - Rischio intermedio (controllo a 3 anni)
3-4 adenomi o almeno 1 adenoma tra i 10 e i 20 mm; o polipi di tipo villoso o con displasia di alto grado. Controllo a 3 anni.
In corso di sorveglianza:
- esame negativo > controllo a 5 anni
- 2 esami negativi > nessuna sorveglianza
- adenomi a basso rischio o rischio intermedio > A
- adenomi ad alto rischio > B
C - Alto rischio (controllo a 1 anno)
5 o più adenomi inferiori ai 10 mm o almeno uno uguale o superiore ai 20 mm.
In corso di sorveglianza:
- esame negativo o adenomi a rischio basso > controllo a 3 anni
- 2 esami negativi consecutivi > controllo a 5 anni
- adenomi a basso rischio o rischio intermedio > A
- adenomi ad alto rischio > C
Per quanto concerne il gruppo a basso rischio è stato dimostrato in recenti studi che il rischio di trovare una neoplasia nei 5 anni successivi in pazienti con 1 o 2 piccoli adenomi tubulari non è significativamente differente dai soggetti in cui non è stato trovato alcun polipo nella colonscopia di base. Per tale motivo questi pazienti non hanno necessità di particolare sorveglianza endoscopica. Al massimo, come suggeriscono le linee guida americane, può essere indicato un controllo a 10 anni.
Accanto agli adenomi, di cui è ben nota la loro storia naturale, l’attenzione degli specialisti si sta concentrando negli ultimi anni su dei polipi con caratteristiche istologiche differenti, ma che ugualmente hanno un rischio di evoluzione tumorale. Si tratta dei polipi serrati.
I polipi serrati del colon retto.
Il polipo serrato, in base a recenti studi, sembra essere responsabile di circa il 20% dei tumori che si riscontrano nel follow up di pazienti sottoposti nei 5 anni precedenti a colonscopia. Si tratta di polipi che seguono una via diversa da quella classica adenoma-carcinoma e che è definita la “via serrata”. Il termine serrato deriva dall’aspetto a “dente di sega” delle cripte dell’epitelio. Tralasciando il dettaglio istologico a letture più specialistiche, ci preme qui sottolineare il fatto che tali lesioni hanno caratteristiche macroscopiche differenti dagli adenomi classici e spesso si confondono con la normale mucosa circostante (Foto 6). Le migliorate conoscenze su tale patologia e le nuove tecnologie endoscopiche (strumenti ad alta definizione, cromoscopia standard o elettronica, ecc.) devono però consentire una più semplice ed immediata diagnosi. Di seguito la loro classificazione e la modalità di sorveglianza in base alle linee guida americane da poco pubblicate.
Polipi iperplastici (HP). Si localizzano al colon distale e retto e usualmente sono di piccole dimensioni (< 5mm) (foto 5). Di colorito chiaro, pallido, tendono ad appiattirsi con l’insufflazione di aria nel colon.
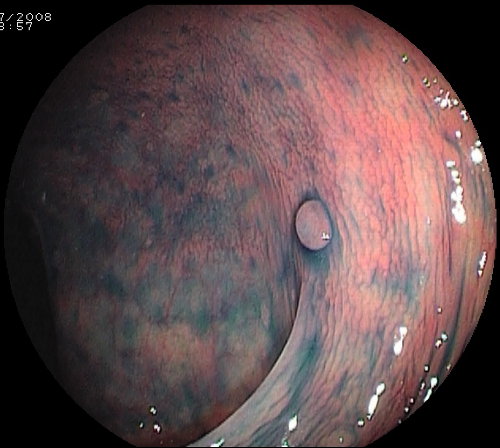
Foto 5: polipo iperplastico del retto dopo colorazione con indaco di carminio
Polipi serrati sessili con o senza displasia (SSA/P). Di solito hanno dimensioni superiori ai polipi iperplastici (nel 50% dei casi superiori a 10 mm), con superficie liscia, regolare, omogenea e spesso non differente dalla mucosa circostante (foto 6 e 7). Sono preferenzialmente localizzati nel colon destro e sono ricoperti da un muco giallastro che consentono di “rivelarsi” all’operatore (attento).
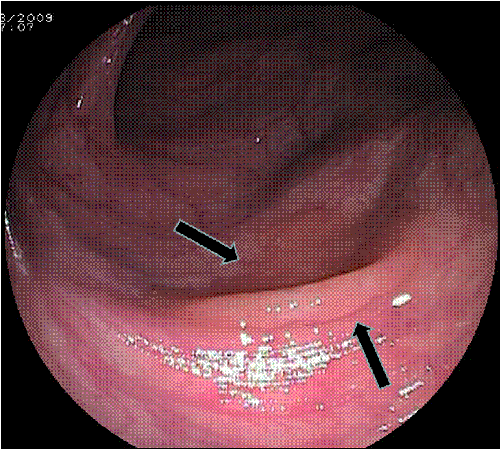
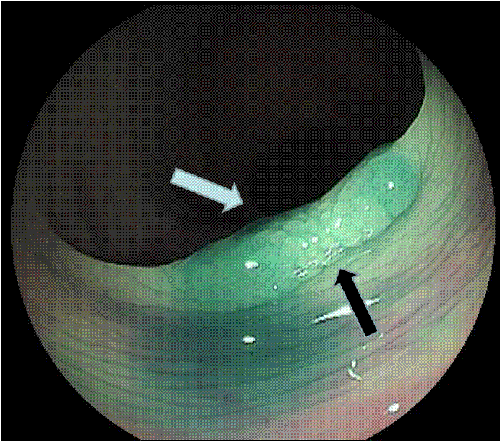
Foto 6: polipo serrato del colon ascendente (poco evidente e di aspetto molto simile alla mucosa circostante) Foto 7: polipo serrato della foto 6 messo in risalto dalla colorazione con indaco di carminio
Adenomi serrati tradizionali (TSA). Con dimensioni che raggiungono i 10 mm, hanno frequentemente un aspetto polipoide ed un’architettura di tipo tubulo-villosa. Si localizzano frequentemente nel colon distale.
Sindrome della poliposi iperplastica. Si tratta di una rara condizione caratterizzata dalla presenza di polipi serrati multipli e/o di grandi dimensioni. Sulla base dei dati disponibili, l’incidenza di cancro colorettale in questi pazienti sembra variare da 40 al 50%. L’Organizzazione Mondiale della Sanità ha indicato i criteri per la diagnosi di questa sindrome.
- presenza di almeno cinque polipi iperplastici situati prossimalmente al sigma, due dei quali con diametro maggiore di 10 mm
- un numero qualsiasi di polipi iperplastici situati prossimalmente al sigma in un individuo che ha una familiarità di primo grado per poliposi iperplastica
- un numero maggiore di 30 polipi iperplastici di qualsiasi dimensione, distribuiti in tutto il colon.
Vengono distinti due tipi di poliposi iperplastiche:
- poliposi iperplastica di tipo I (poliposi serrata adenomatosa), caratterizzata da molteplici (cinque o più) adenomi sessili serrati, di grandi dimensioni, situati a livello del colon prossimale (coesistenti con adenomi serrati tradizionali, polipi misti, e adenomi convenzionali) associata ad un rischio significativo di trasformazione carcinomatosa
- poliposi iperplastica di tipo II, condizione più eterogenea, caratterizzata dalla presenza di numerosi (≥ 30) piccoli polipi iperplastici distribuiti in tutto il colon, e con un’associazione significativamente più debole con il cancro colo rettale.
Il 50% dei pazienti con poliposi iperplastica presenta una storia familiare di cancro al colon (condizione non su base ereditaria, ma genetica).
Sorveglianza dei polipi serrati
Caratteristiche dei polipi Sorveglianza endoscopica raccomandata (anni)
| Polipi iperplastici piccoli (< 10 mm) al retto e sigma | 10 |
| Meno di 3 polipi serrati inferiori ai 10 mm senza displasia | 5 |
| Polipi serrati sessili grandi (< 10 mm) | 3 |
| Meno di 3 polipi serrati sessili | 3 |
| Polipi serrati sessili con displasia | 1-3 |
| Adenoma serrato sessile | 3 |
| Poliposi iperplastica di tipo I | 1 |
Altri concetti fondamentali
Durata dei controlli
Non è semplice stabilire un limite alla sorveglianza ma le società scientifiche indicano l'età di 85 anni oltre il quale i rischi della colonscopia superano i benefici. Per i pazienti fra i 75 e gli 85 anni la decisione di continuare la sorveglianza dovrà essere valutata singolarmente tenendo conto delle caratteristiche dei polipi rimossi, delle eventuali malattie associate e dell'aspettattiva di vita del paziente.
Comparsa di nuovi sintomi in corso della sorveglianza
La comparsa di sintomi sospetti deve essere tenuta in considerazione e adeguatamente valutata. Come si è detto la colonscopia riduce il rischio di neoplasia avanzata ma non lo elimina completamente per i motivi già esposti all’inizio.
Ruolo del sangue occulto
In base alle linee guida non vi è razionale e beneficio a ricercare il sangue occulto in corso di sorveglianza endoscopica.
Cancro pT1
Il carcinoma infiltrante la sottomucosa (pT1) rappresenta la forma più precoce di adenocarcinoma e se il trattamento endoscopico è stato ritenuto idoneo come soluzione della patologia, va inserito come sorveglianza nel gruppo delle lesioni ad alto rischio (classe C).
Colonscopia di qualità
La colonscopia di base costituisce il punto cruciale della sorveglianza dei pazienti a rischio. Tale esame è una procedura di grande “responsabilità” da parte dell’endoscopista: una sua disattenzione, con mancata visualizzazione di una lesione, può essere fatale per il paziente. Per tale motivo bisogna che l’endoscopista rispetti le regole fondamentali nella procedura, già indicate dalle società scientifiche.
E’ fondamentale sapere che una colonscopia anche se completa può non avere un’efficacia del 100%. La “dimenticanza” per adenomi inferiori ai 10 mm varia infatti dal 25 al 50%, ma la cosa più grave è che in base ad alcuni recenti studi fino al 6% degli adenomi superiori ai 10 mm e circa il 4% dei cancri non viene identificato dalla colonscopia..
Ecco dunque l’esigenza di una tecnica adeguata.
- L’esame deve essere eseguito in condizioni ottimali di pulizia intestinale (Foto 8,9,10) e deve essere condotto fino all’esplorazione del fondo ciecale e della visualizzazione della valvola ileo-ciecale e del forame appendicolare. In caso di esame non completo (per cattiva toilette intestinale, particolare anatomia del colon, aderenze intestinali, ecc.) l’esplorazione deve essere ripetuta (soprattutto se il paziente fa parte di un gruppo a rischio) eventualmente facendo riferimento anche alle metodiche alternative (colonscopia TAC, colonscopia robotica, videocapsula).
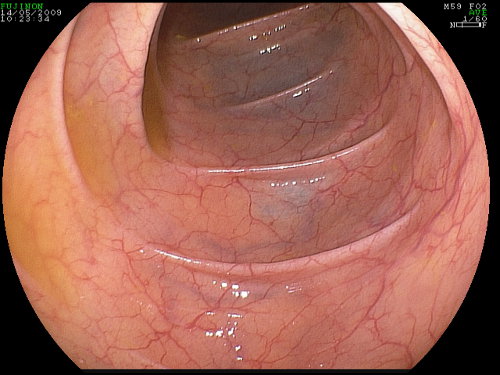
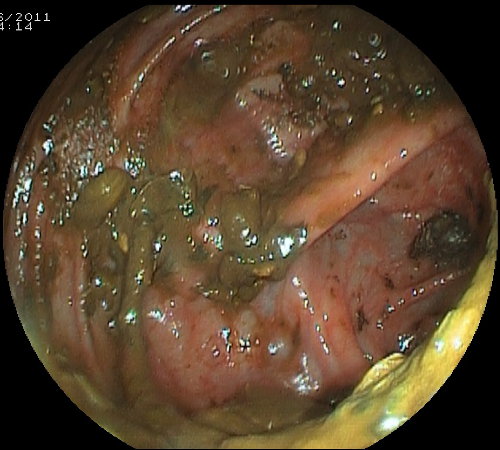
Foto 8: condizioni ottimali di pulizia - Foto 9: pulizia intestinale inadeguata per la presenza di materiale fecale
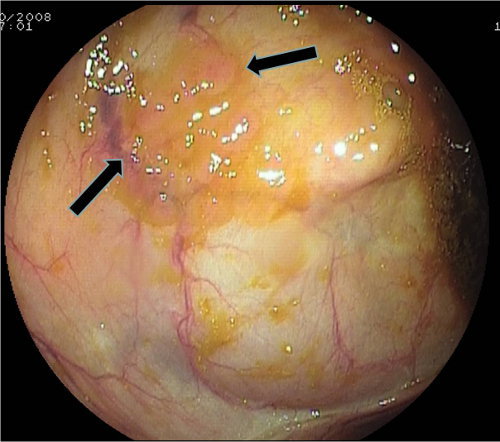
Foto 10: polipo piatto nascosto dal materiale fecale
- La colonscopia deve essere condotta in sedazione (cosciente) in modo che l’esame risulti accettabile per il paziente e possa consentire all’operatore di lavorare nelle condizioni ottimali. E' stato inoltre dimostrato che una colonscopia in sedazione consente un più facile raggiungimento del cieco 8 e, quindi, di essere completa).
- Bisogna prestare la massima attenzione in caso di rimozione di grossi adenomi sessili o a larga base ed accertarsi con controlli ravvicinati della completa guarigione e dell'assenza di adenoma residuo (Foto 11). Infatti, circa il 25% dei cancri individuati entro 3 anni da una colonscopia completa si sviluppa proprio nella sede di una precedente polipectomia incompleta. Tali lesioni devono essere riviste dopo 3 mesi ed il tessuto residuo dovrà essere trattato (Foto 12). Da considerare, in presenza di grosse formazioni polipose, l'opzione chirurgica o l’invio del paziente verso Centri di endoscopia di provata esperienza.
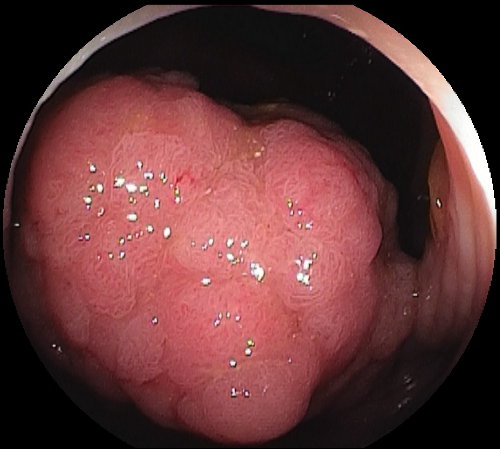
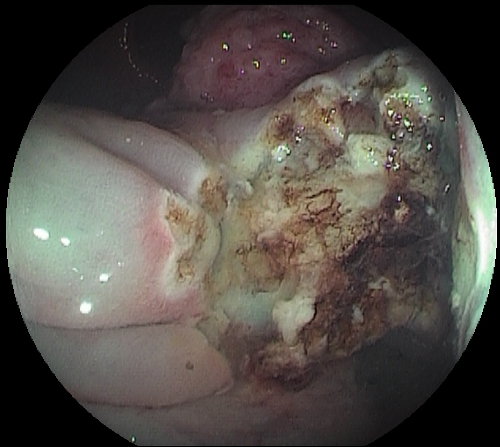
Foto 11: grosso polipo sessile della flessura epatica - Foto 11a: base del polipo dopo la sua rimozione completa
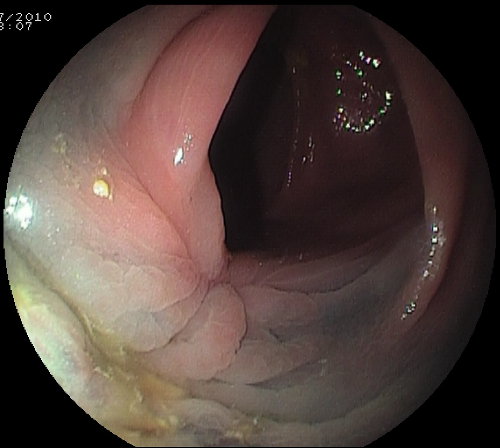
Foto 11b: il controllo a 3 mesi dimostra la completa cicatrizzazione della base e l’assenza di tessuto residuo.
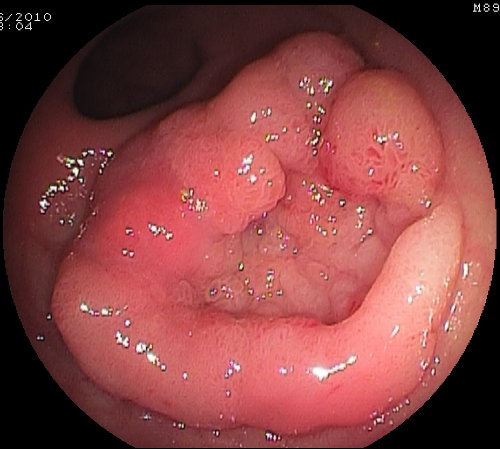
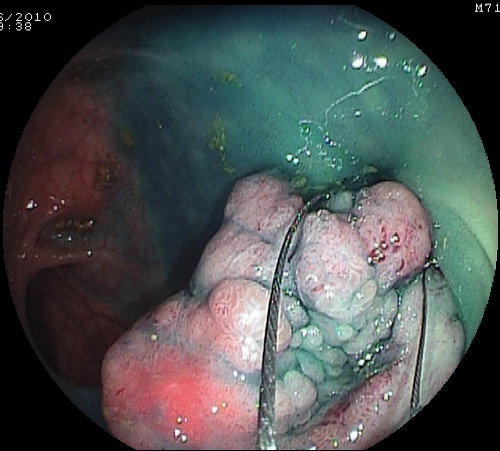
Foto 12: adenoma piatto-rilevato del colon ascendente - Foto 12 a: fase della rimozione con ansa diatermica
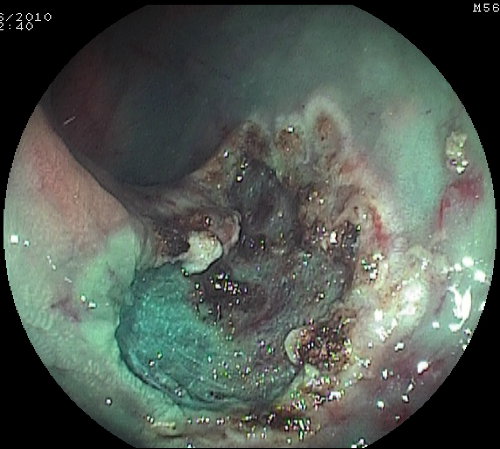
Foto 12b: base del polipo dopo la sua completa rimozione
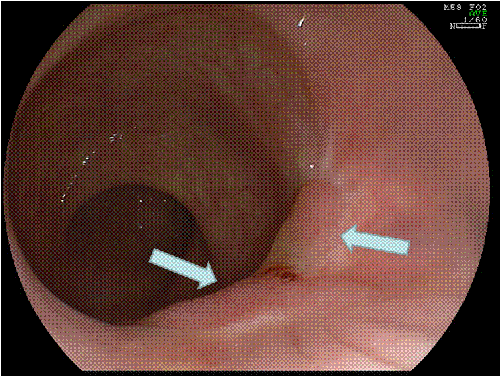
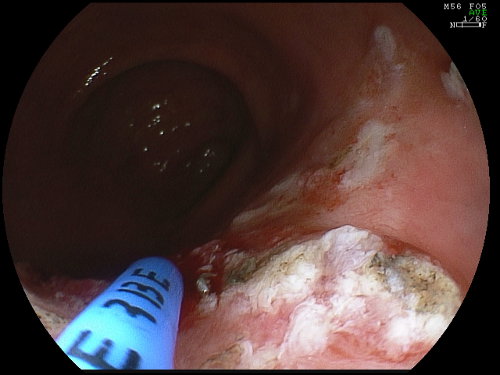
Foto 12c: il controllo a tre mesi mette in evidenza la cicatrice, ma con presenza di tessuto adenomatoso residuo - Foto 12d: il tessuto residuo viene definitivamente distrutto mediante elettrocoagulazione con Argon Plasma Coagulation (APC). Il successivo controllo a 3 mesi ha rilevato la completa guarigione.
Per approfondire:
- Segnan N.: European guidelines for quality assurance in colorectal cancer screening and diagnosis, European Commission, Publication Office of the European Union; 2010.
- Liberman DA: Guidelines for Colonscopy Surveillance after Screening and Polypectomy (AGA Commission); Gastroenterology 2012; 143:844-857
- Atkin WS: European Guidelines for quality assurance in colorectal cancer screening and diagnosis. Colonscopy surveillance following adenoma removal. Endoscopy 2012;44: 151-163
- La colonscopia di qualità
- Cancro del colon-retto: prevenzione primaria e secondaria
- Il polipo maligno (cancerizzato) del colon
- La nuova colonscopia robotica: indolore, senza complicanze, operativa e monouso