La malattia celiaca: nuovo marker per la diagnosi
La malattia celiaca: cos'è, come si manifesta, come si diagnostica e si cura
COS'E'
La celiachia o malattia celiaca (MC) è definita dall'ESPGHAN del 2012 come un disordine sistemico immunomediato provocato, in soggetti geneticamente predisposti, dall'ingestione di glutine che si forma durante la lavorazione delle farine (lipoproteina composta da due tipi di proteine: le gluteline e le prolammine) presente in alcuni cereali (frumento, segale, orzo, farro).
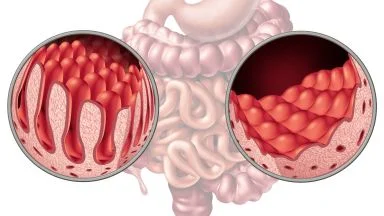
Nei soggetti predisposti quindi l'ingestione del glutine provoca gravi danni a livello della mucosa intestinale, la quale viene attaccata dagli anticorpi prodotti dall'organismo stesso; il danneggiamento della mucosa provoca a sua volta una severa diminuzione della capacità di assorbimento intestinale, che a lungo andare provocherà sintomi e segni della patologia.
Il danno mucosale è caratterizzato da atrofia dei villi duodenali e digiunali associato ad una iperplasia delle cripte con un ricco infiltrato di cellule linfocitarie (B e T) sia tra gli enterociti che nella lamina propria dei villi intestinali. Tali alterazioni sono reversibili, con ripristino della normale morfologia della mucosa, eliminando completamente il glutine dalla dieta.
CHI SI AMMALA?
Tutte le persone geneticamente predisposte. Può comparire a qualsiasi età. L'incidenza in Italia è stimata 1:100/150, mentre la prevalenza è di circa 1%. Purtroppo ancora in Italia solo una parte di questi soggetti è consapevole della malattia, infatti i celiaci noti sono poco più di 70.000 contro un numero reale stimato in circa 500.000. La frequenza delle diagnosi è in aumento grazie alla crescente applicazione dei test diagnostici nella pratica clinica, ciò nonostante il 70-80% dei casi sfuggono alla diagnosi.
QUALI SONO LE CAUSE
La presenza di una forte componente genetica è dimostrata da:
- l'elevata prevalenza nei parenti di 1° grado (il 10-12% circa dei familiari di 1° grado dei soggetti celiaci è affetto, con un rischio di almeno 20 volte maggiore di quello della popolazione generale
- il tasso di concordanza tra gemelli monozigoti (82%) è maggiore di quello dei gemelli dizigoti (13%)
- il coinvolgimento dei geni del sistema HLA nella suscettibilità verso la malattia.
Comunque i dati epidemiologici a disposizione suggeriscono una genesi multifattoriale, cioè oltre ai fattori genetici esiste una forte componente ambientale. Infatti il glutine introdotto nella dieta, in soggetti geneticamente predisposti provoca le alterazioni mucosali sopra descritti con il conseguente malassorbimento di vari nutrienti.
Tra i fattori ambientali il glutine rappresenta quello più importante.
QUALI SONO I SINTOMI
La sintomatologia può essere variegata tanto da dare diversi sintomi riguardanti sia l'apparato digerente che altri organi ed apparati e può svilupparsi in fasi diverse della vita.
Vengono distinti diverse forme cliniche:
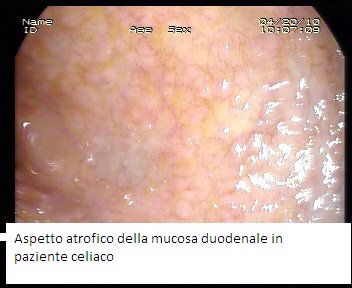
- Forma classica o tipica: a esordio dopo lo svezzamento (6-24 mesi di vita), dopo l'introduzione del glutine nella dieta. Il bambino presenta i sintomi tipici del malassorbimento quali: scarsa crescita, diarrea cronica, distensione addominale, astenia, ipotonia muscolare,inappetenza, irritabilità. Da un punto di vista endoscopico la mucosa digiunale appare piatta per atrofia dei villi.
- Forma non classica o atipica: si presenta in età scolare con sintomi atipici come: dolori addominali ricorrenti, stipsi o manifestazioni extraintestinali come: bassa statura,ritardo puberale, anemia sideropenica, alopecia, stomatite aftosa, osteoporosi, difetti dello smalto dentario. miocardite autoimmune, aumento delle transaminasi.
- Forma silente: si riscontra in soggetti apparentemente sani con mucosa intestinale leggermente danneggiata che regredisce con dieta aglutinata. E' una forma asintomatica riscontrata nei soggetti sottoposti a screening in quanto parenti di 1° grado di pazienti celiaci o diabetici di tipo I.
- Forma potenziale o latente: si riscontra nei soggetti geneticamente predisposti con esami sierologici positivi ma biopsia intestinale normale. Questi sono i pazienti che devono essere controllati e monitorati negli anni per valutare l'evoluzione.
- Forma refrattaria: si ha quando il paziente no risponde alla dieta aglutinata ed è presente dal 2 al 5% dei celiaci. Se ne distinguono due forme: una primaria se il paziente non risponde fin dall'inizio alla dieta aglutinata e l'altra secondaria caratterizzata da una prima risposta positiva alla dieta aglutinata e una successiva fase di non risposta con persistenza dell'atrofia della mucosa dopo almeno 15 mesi di dieta aglutinata.
Si riconoscono due forme di MCR:
- MCR di tipo 1 con normale fenotipo di IEL (CD3+ e CD8+), con risposta clinica alla terapia con immunosoppressori e basso rischio di linfoma
- MCR di tipo 2 con fenotipo aberrante di IEL (CD3-; CD8-) con minima e transitoria o assente risposta clinica alla terapia con immunosoppressori ed alto rischio di linfoma T.
Nei pazienti con MC non responsiva o refrattaria e necessaria una valutazione attenta e il trattamento della specifica etiologia.
In questi casi, i primi passi sono costituiti dalla valutazione sierologia e dalla rigorosa verifica della dieta da parte di un dietologo esperto (Raccomandazione forte, livello di evidenza elevato).
COME SI FA DIAGNOSI
Si inizia con un'accurata anamnesi e successivamente nei casi sospetti si eseguono gli esami strumentali necessari, primi fra tutti il dosaggio degli anticorpi (anticorpi transglutaminasi, antigliadina ed antiendomisio), successivamente si esegue la biopsia duodenale tramite esofagogastroduodenoscopia nei soggetti con anticorpi positivi.
Anticorpi Antipeptidi Deamidati di Gliadina (DGP-AGA): La diagnostica sierologica della celiachia si è arricchita recentemente di un nuovo interessante marcatore, rappresentato dagli Anticorpi Antipeptidi deamidati di gliadina DGP-AGA. La sensibilità di questo test è pari all’84% sia per gli anticorpi di classe IgA che IgG, e presenta un’elevata specificità per la classe IgG (99%).
Il confronto fra questo nuovo anticorpo ed i test tradizionali ha mostrato che i DGP-AGA hanno un’accuratezza diagnostica marcatamente più elevata di quella dei tradizionali AGA; inoltre, sebbene i DGP-AGA mostrino una sensibilità inferiore rispetto agli EMA e agli anti-tTG, la loro specificità per la classe IgG è cosi elevata da raggiungere quella degli EMA IgA e da superare quella degli anti-tTG IgA.
Può essere prospettata pertanto una futura strategia anticorpale basata sulla determinazione combinata di anti-tTG IgA e DGP-AGA IgG. In questo modo i DGP-AGA IgG consentirebbero non solo di confermare la specificità degli anti-tTG ma anche di identificare la presenza di celiachia nei pazienti con deficit di IgA.
Inoltre, sebbene i DGP-AGA di classe IgG si siano rivelati un eccellente marcatore anticorpale per identificare i celiaci al di sotto dei due anni di età, tuttavia il test DGP-AGA di classe IgA sembra essere ancora più sensibile in questa fascia d’età; pertanto per non perdere pazienti dovrebbero essere eseguite entrambe le deamidate.
Nel monitoraggio della MC gli Anti-TTG e i DGP-AGA hanno mostrato la stessa accuratezza diagnostica nel predire lo stato della mucosa intestinale dopo dieta aglutinata; la loro persistenza infatti è significativamente associata con la mancanza di miglioramento della mucosa intestinale mentre la loro scomparsa è espressione di recupero della stessa. Inoltre nei bambini che seguono una dieta aglutinata, il test DGP- AGA IgA sembra essere più utile rispetto al test Anti-TTG IgA poiché si negativizza prima e si positivizza prima nel momento in cui c’è una ripresa della dieta libera
Una eccezione è rappresentato dal bambino con sintomi altamente suggestivi per malattia celiaca per il quale le recenti linee guida ESPGHAN ritengono non più necessaria la biopsia duodenale qualora gli anticorpi tTg-IgA siano 10 volte superiori al avlore di riferimento, gli anticorpi anti-endomisio siano positivi e la tipizzazione HLA sia compatibile con la MC.
COME SI CURA
Ad oggi l'unico trattamento efficace è alimentarsi con prodotti privi di glutine per migliorare le condizioni della mucosa intestinale ed eliminare il malassorbimento che ne consegue; ciò permette quindi di eliminare i sintomi e prevenire le complicanze.
COMPLICANZE
La complicanze che desidero attenzionare, ma non è l'unica, è il rischio di tumore intestinale che è 50 volte superiore a quello della popolazione generale se un paziente celiaco continua a mangiare glutine.
FONTI E CITAZIONI BIBLIOGRAFICHE
- Diagnostica e sierologia della celiachia: U.Volta. SIMG 3-2007
- Old and new serological tests for celiac disease screening: U.Volta er al. Expert Rev.Gastroenterolo Hepatol 2010; 4:31-5
- WGO Global Guidelines - Celiac disease - World Gastroenterology Organisation 2012
- Biagi er al 2012 J.Clin Gastroenterolo 46, 46-50
- ACG Clinical Guidelines: Diagnosis and Management of Celiac Disease
- Giorn.Ital.End.Dig. 2014; 37:177-181